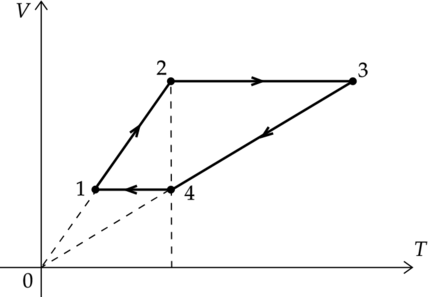
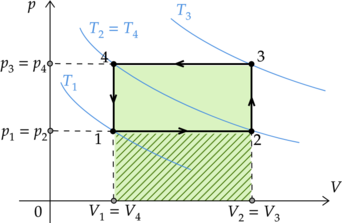
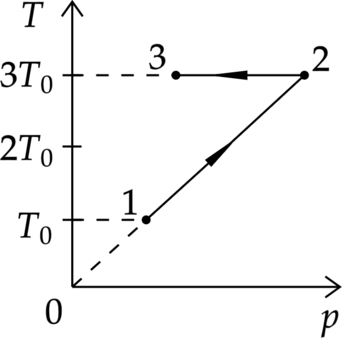
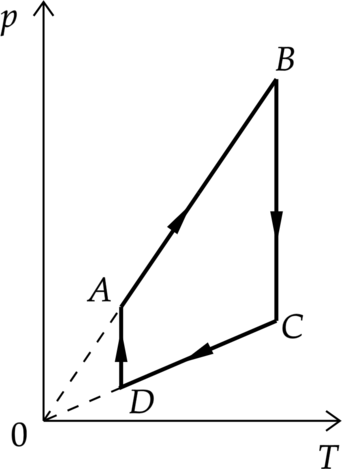
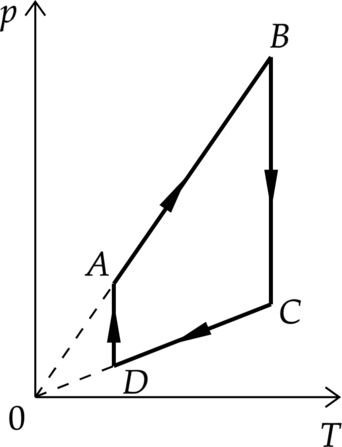
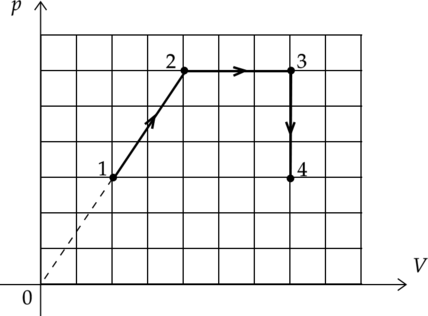
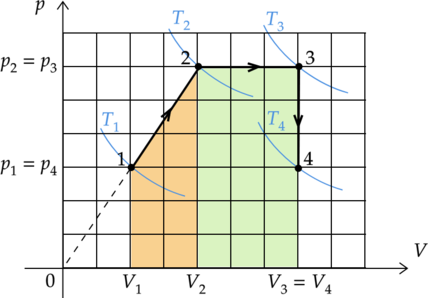
На рисунке изображена диаграмма циклического процесса. Выберите из предложенных утверждений два верных:
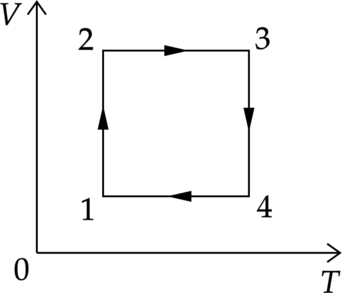
1) На участке 1–2 внутренняя энергия газа увеличивается.
2) На участке 2–3 газ совершает положительную работу.
3) На участке 3–4 давление газа увеличивается.
4) На участке 2–3 газу сообщили некоторое количество теплоты.
5) Внутренняя энергия газа в состоянии 1 больше, чем внутренняя энергия газа в состоянии 3.
“Досрочная волна 2019 вариант 2”
1) Поскольку на участке 1–2 температура была постоянной, следовательно, внутренняя энергия газа не изменилась.
Утверждение 1 – \(\color{red}{\small \text{Неверно}}\)
2) Поскольку на участке 2–3 объём газа оставался неизменным, следовательно, работа не совершалась.
Утверждение 2 – \(\color{red}{\small \text{Неверно}}\)
3) Поскольку на участке 3–4 температура оставалась постоянной, а объём уменьшился, при этом \(pV = const\), значит, давление возросло.
Утверждение 3 – \(\color{green}{\small \text{Верно}}\)
4) Поскольку на участке 2–3 объём газа не изменялся, работа не совершалась, но при этом возросла температура, значит, изменение внутренней энергии положительно.
Утверждение 4 – \(\color{green}{\small \text{Верно}}\)
5) Поскольку температура в состоянии 1 меньше, чем в состоянии 3, значит, и внутренняя энергия в состоянии 1 меньше.
Утверждение 5 – \(\color{red}{\small \text{Неверно}}\)
Ответ: 34