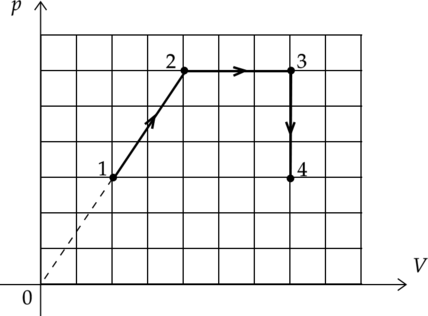
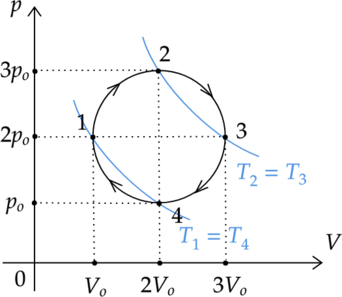
На рисунке показан график циклического процесса, проведенного с одноатомным идеальным газом, в координатах \(p-V\), где \(p\) — давление газа, \(V\) — объем газа. Количество вещества газа остается неизменным.
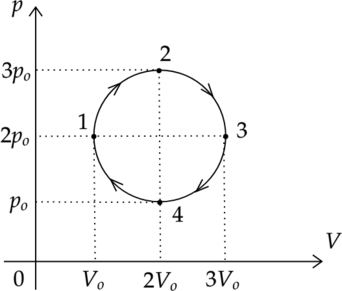
Из приведенного ниже списка выберите два правильных утверждения, характеризующих процессы на графике.
1) Внутренняя энергия газа в состоянии 3 больше, чем в состоянии 1.
2) В процессе 1-2 газ отдал положительное количество теплоты в окружающую среду.
3) Внешние силы в процессе 4-1 совершили большую работу, чем совершил газ в процессе 2-3.
4) Газ за цикл совершил положительную работу.
5) В процессе 3-4 внутренняя энергия газа постоянна.
1) \(\color{green}{\small\text{Верно }}\)
Внутренняя энергия газа зависит от его температуры: \[U = \frac{3}{2}\nu RT,\] где \(\nu\) — количество вещества газа, \(R\) — универсальная газовая постоянная.
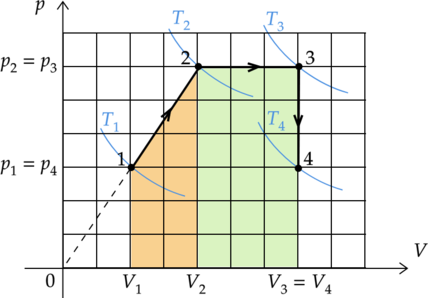
Проведем две изотермы. По рисунку видно, что изотерма \(T_3\) лежит ”выше”, чем изотерма \(T_1\): \(T_3 > T_1\). Следовательно, внутренняя энергия газа в состоянии 3 больше, чем в состоянии 1.
2) \(\color{red}{\small\text{Неверно }}\)
Запишем первый закон термодинамики для процесса 1-2: \[Q_{3-4} = A'_{1-2} + \Delta U_{1-2}\] Работа газа зависит от изменения его объема: \[A'_{1-2} = p \Delta V\] По графику видно, что объем газа в процессе 1-2 увеличивается. Следовательно, газ совершил положительную работу.
Изменение внутренней энергии газа зависит от температуры: \[\Delta U = \frac{3}{2} \nu R\Delta T\] Так как изотерма \(T_2\) лежит ”выше” изотермы \(T_1\), то \(T_2 > T_1\). Cледовательно, изменение температуры положительно: \(\Delta T = T_2 - T_1 > 0\). Следовательно, и изменение внутренней энергии \(\Delta U_{1-2}\) также положительно.
Так как изменение внутренней энергии газа и его работа положительны, то и количество теплоты \(Q_{1-2}\) также положительно. Значит, газ не отдает тепло в окружающую среду, а получает его.
3) \(\color{red}{\small\text{Неверно }}\)
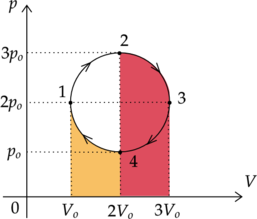
Работу газа и работу внешних сил можно найти как площади под графиком процессов 4-1 и 2-3. Видно, что площадь под графиком процесса 4-1 меньше, чем под графиком процесса 2-3. Следовательно, внешние силы в процессе 4-1 совершили меньшую работу, чем совершил газ в процессе 2-3.
4) \(\color{green}{\small\text{Верно }}\)
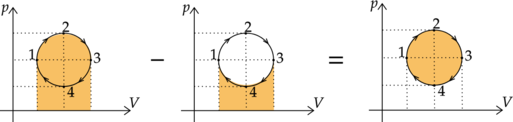
Работа \(A_\text{ц}\), совершенная газом за цикл, равна площади, заключенной внутри кривой 1-2-3-4-1.
Работа, совершенная газом в процессе 1-2-3, положительна и равна площади под графиком, а работа, совершенная в процессе 3-4-1, отрицательна и также равна площади под графиком.
Суммарная работа равна разности этих двух площадей и, следовательно, равна площади внутри замкнутой кривой, изображающей цикл. Так как объем газа увеличился, то его работа за цикл положительна.
5) \(\color{red}{\small\text{Неверно }}\)
Изменение внутренней энергии газа зависит от изменения его температуры: \[\Delta U = \frac{3}{2}\nu R\Delta T,\] где \(\nu\) — количество вещества газа, \(R\) — универсальная газовая постоянная.
По рисунку видно, что изотерма \(T_4\) лежит ”ниже”, чем изотерма \(T_3\): \(T_4 < T_3\). Следовательно, внутренняя энергия газа в состоянии 4 меньше, чем в состоянии 3: \(\Delta T = T_4 - T_3 < 0\).
Ответ: 14