Одно и то же постоянное количество одноатомного идеального газа расширяется из одного и того же начального состояния \(p_1\), \(V_1 \) до одного и того же конечного объёма \(V_2\) первый раз по изобаре 1–2, а второй – по адиабате 1–3 (см. рисунок). Отношение количества теплоты \(Q_{12}\), полученного газом от нагревателя в ходе процесса 1–2, к модулю изменения внутренней энергии газа в ходе процесса 1–3 равно k = 5. Определите отношение \(\dfrac{A_{12}}{A_{13}}\) работы газа в процессе 1–2 к работе газа в процессе 1–3.
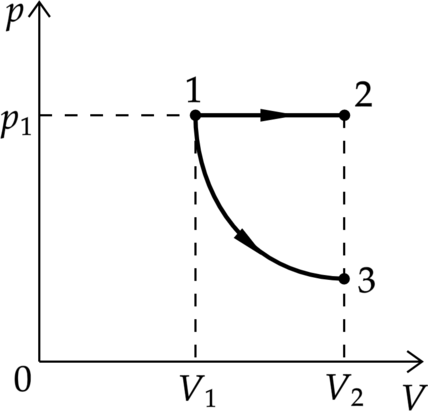
Запишем уравнение Клапейрона–Менделеева \[pV=\nu RT\] По первому закону термодинамики количество теплоты, полученное телом в процессе 1–2 равно \[Q=\Delta U +A,\] где \(Q\) – количество теплоты, полученное системой, \(\Delta U\) – изменение внутренней энергии системы, \(A\) – работа газа.
Или с учетом уравнения Клапейрона–Менделеева \[Q_{12}=U_2-U_1+A=\dfrac{3}{2}\left(\nu RT_2-\nu R T_1\right)+ p_1 \left(V_2-V_1\right) =\dfrac{3}{2} p_1 \left(V_2-V_1\right)+ p_1 \left(V_2-V_1\right)=\dfrac{5}{2} p_1 \left(V_2-V_1\right)=\dfrac{5}{2}A_{12}\] Процесс 1–3 адиабатный, значит, работа газа равна \[A_{13}=|\Delta U{13}|=|U_3-U_1|\] \[\dfrac{A_12}{A_13}=\dfrac{2}{5}\cdot \dfrac{Q_{12}}{|U_3-U_1|}=\dfrac{2}{5}\cdot 5 =2\]
Ответ: 2



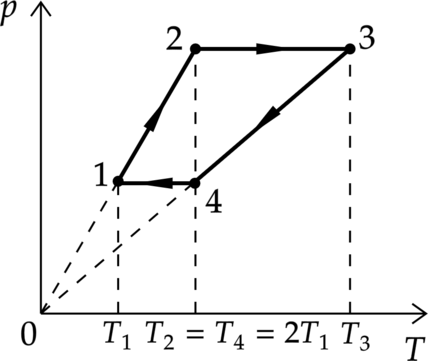
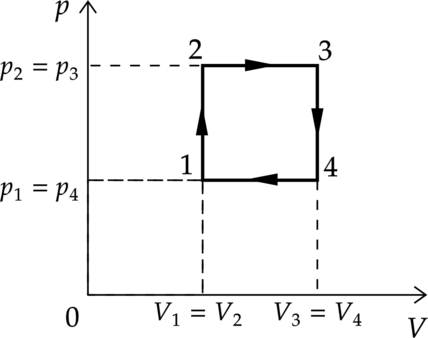 3. Проанализируем график, цикл состоит из двух изохор, 1-2 и 3-4, и двух изобар, 2-3 и 4-1 (см. рисунок цикла в координатах p-V).
3. Проанализируем график, цикл состоит из двух изохор, 1-2 и 3-4, и двух изобар, 2-3 и 4-1 (см. рисунок цикла в координатах p-V).